“Bioactive Ceria Nanoenzymes Target Mitochondria in Reperfusion Injury to Treat Ischemic Stroke”
DOI: 10.1021/acsnano.3c10982

摘要
本研究开发了一种新型的靶向线粒体的纳米递送系统TPP@(CeO2+ROF),旨在治疗缺血性中风。该系统基于氧化铈纳米酶(CeNZs)和罗氟司特(ROF)的协同作用,并采用三苯基膦(TPP)进行修饰,以提高其靶向性和生物利用度。体外实验表明,该纳米递送系统具有良好的抗氧化活性,能够有效清除ROS。在PC12细胞模型中显示,该纳米递送系统能够有效保护PC12细胞免受氧化应激和细胞凋亡的损伤,并改善线粒体功能。在MCAO大鼠模型中表明该纳米递送系统能够靶向脑梗死区域,并降低梗死体积、改善氧化应激和炎症反应,以及增强神经功能。此外,该纳米递送系统还能够调节MCAO大鼠模型中微胶质细胞的表型,从促炎M1型转化为抗炎M2型,从而抑制炎症反应,促进神经修复。
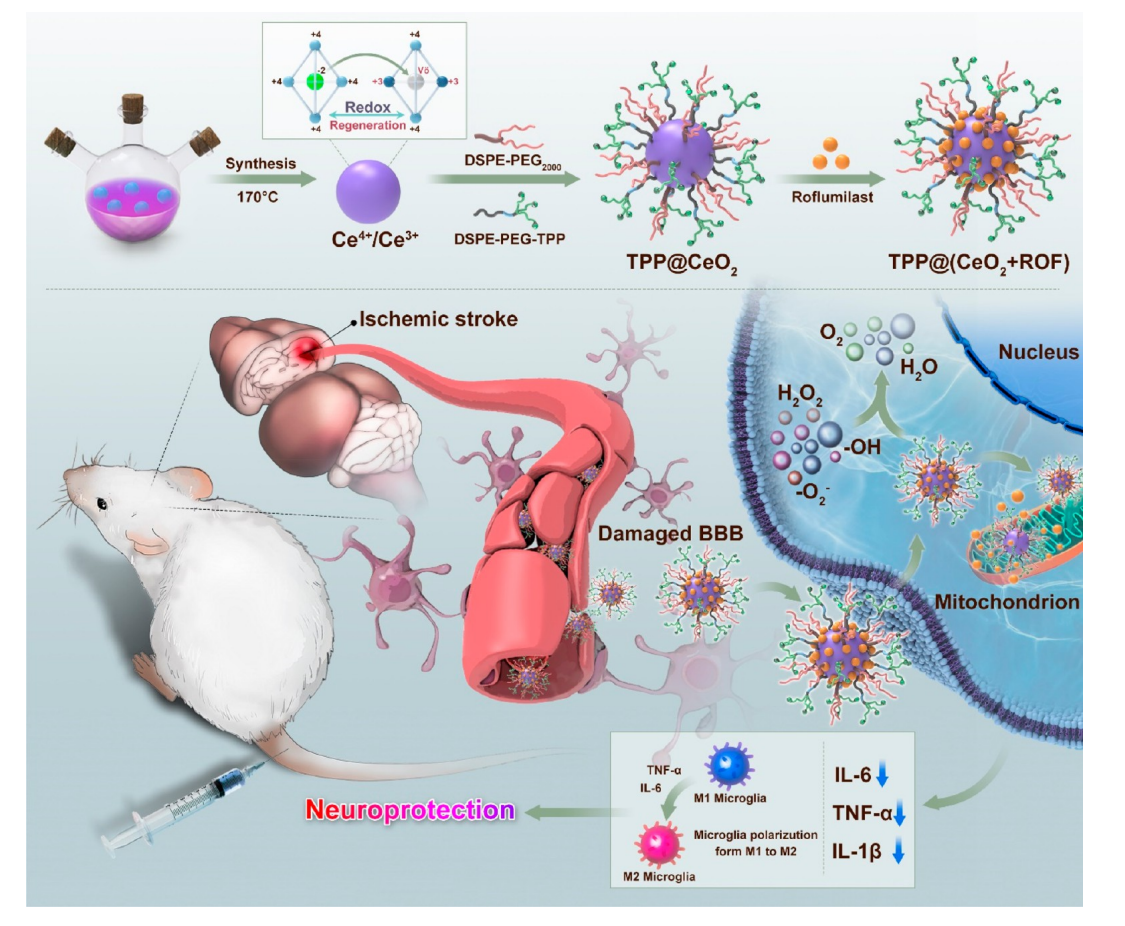
靶向线粒体的氧化铈纳米酶治疗缺血性脑卒中的示意图
背景
缺血性中风是全球主要的健康问题,主要治疗方法为静脉注射重组组织型纤溶酶原激活剂(rt-PA),但存在治疗时间限制和副作用等问题。针对以上问题,研究人员提出了靶向线粒体的治疗策略。线粒体是细胞的“能量工厂”,在缺血性中风发生后,线粒体功能会受损,导致细胞能量平衡紊乱、神经元功能障碍和活性氧(ROS)产生与清除失衡。过量的ROS会导致氧化应激,损害细胞成分,并激活炎症反应,最终导致神经元死亡。铈纳米酶(CeNZs)具有调节活性氧(ROS)的特殊性质,可以模拟超氧化物歧化酶(SOD)和过氧化氢酶(CAT)的活性,从而清除活性氧(ROS)并减轻氧化应激。因此,靶向线粒体、减轻氧化应激和调节炎症反应,是治疗缺血性中风的关键。纳米材料在实现靶向治疗方面具有巨大的潜力,而具有酶模拟活性的纳米酶,如氧化铈纳米酶(CeNZs),则能够有效地调节活性氧(ROS)水平,并具有高效率和可重复性等优点。
研究亮点
(1)使用三苯基膦(TPP)对铈纳米酶(CeNZs)进行修饰,使纳米系统能够精准地靶向线粒体,从而更有效地调节线粒体功能,减轻氧化应激和炎症反应,改善缺血微环境。
(2)使用1,2-二硬脂酰基-sn-丙三基-3-磷脂酰乙醇胺(DSPE)对铈纳米酶(CeNZs)进行包裹,提高纳米系统在血液循环中的稳定性,并减少免疫系统的捕获,从而增强其生物利用度。
(3)将第四代PDE4抑制剂罗氟司特(ROF)负载到TPP@CeO2中,与CeNZs协同作用,增强纳米系统神经保护效果。
(4)TPP@(CeO2+ROF)能够将激活的小胶质细胞从促炎M1型转变为抗炎M2型,从而调节炎症反应,减轻神经损伤。
(5)RNA测序分析表明,TPP@(CeO2+ROF)可以通过影响TGF-β信号通路和GPCR信号通路,降低炎症水平并促进神经发育。
图文欣赏
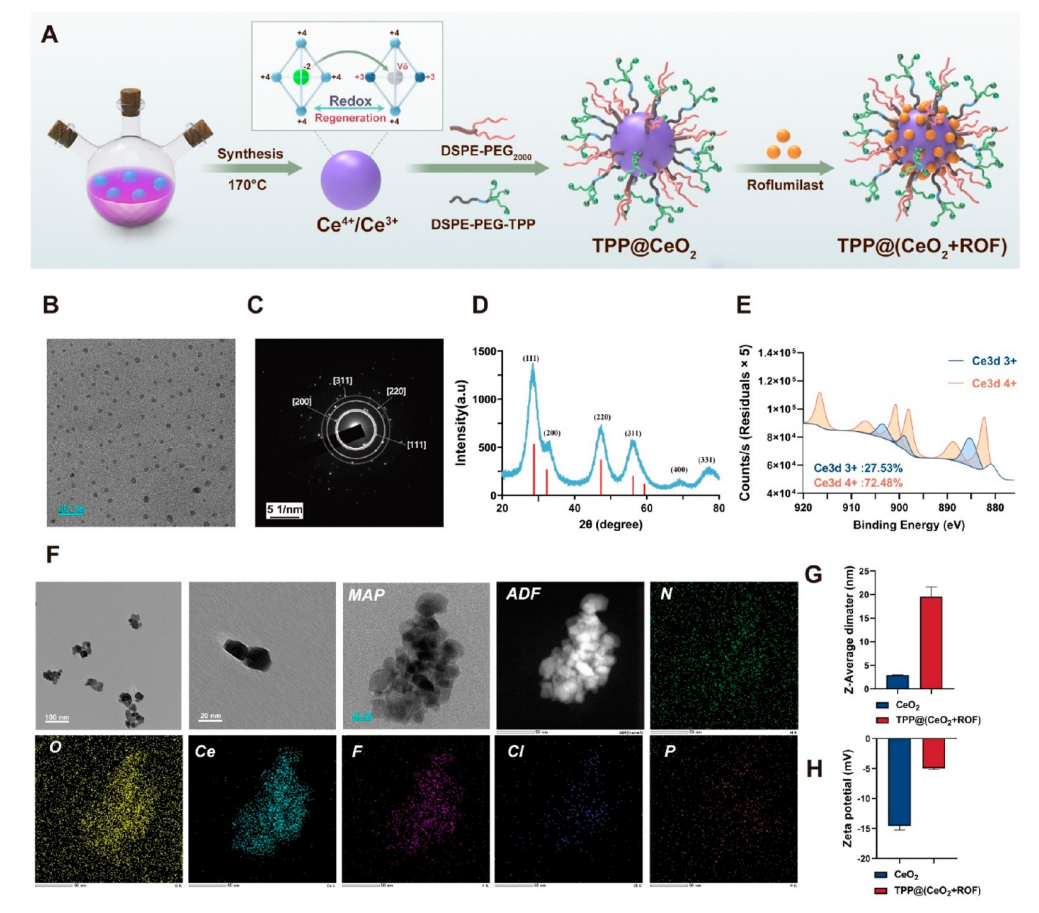
图1.TPP@(CeO2+ROF)的合成与表征
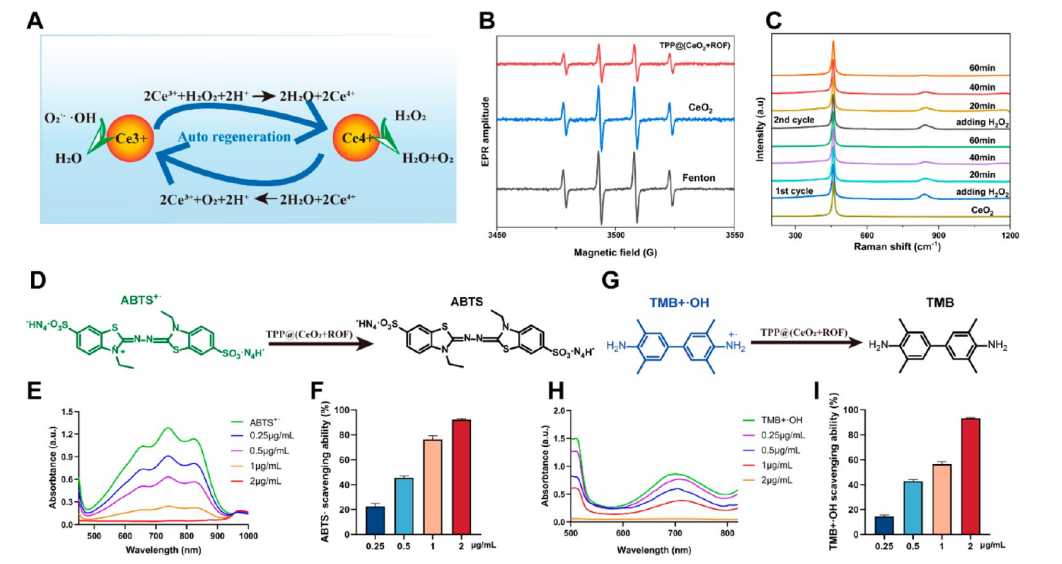
图2.TPP@(CeO2+ROF)体外清除自由基的研究
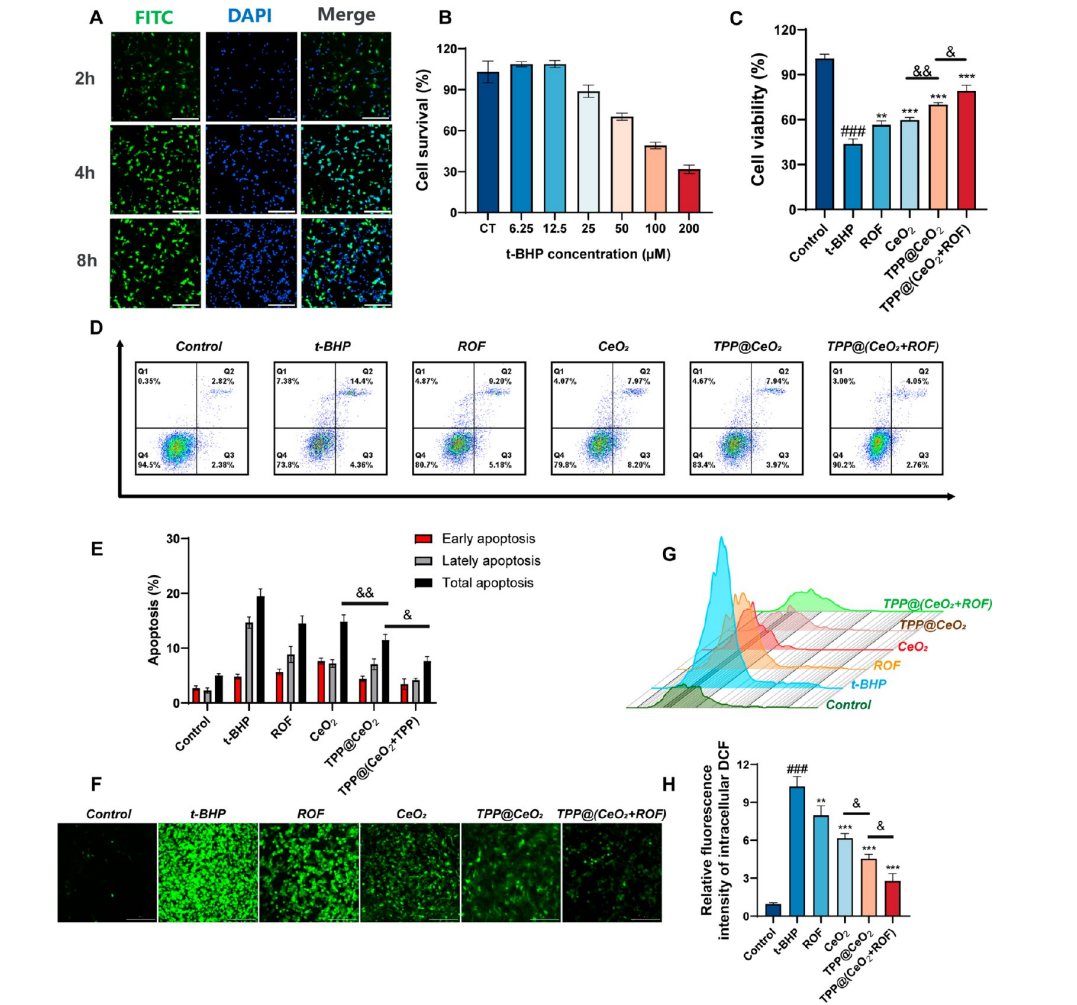
图3.TPP@(CeO2+ROF)保护t-BHP诱导的PC12细胞氧化应激损伤
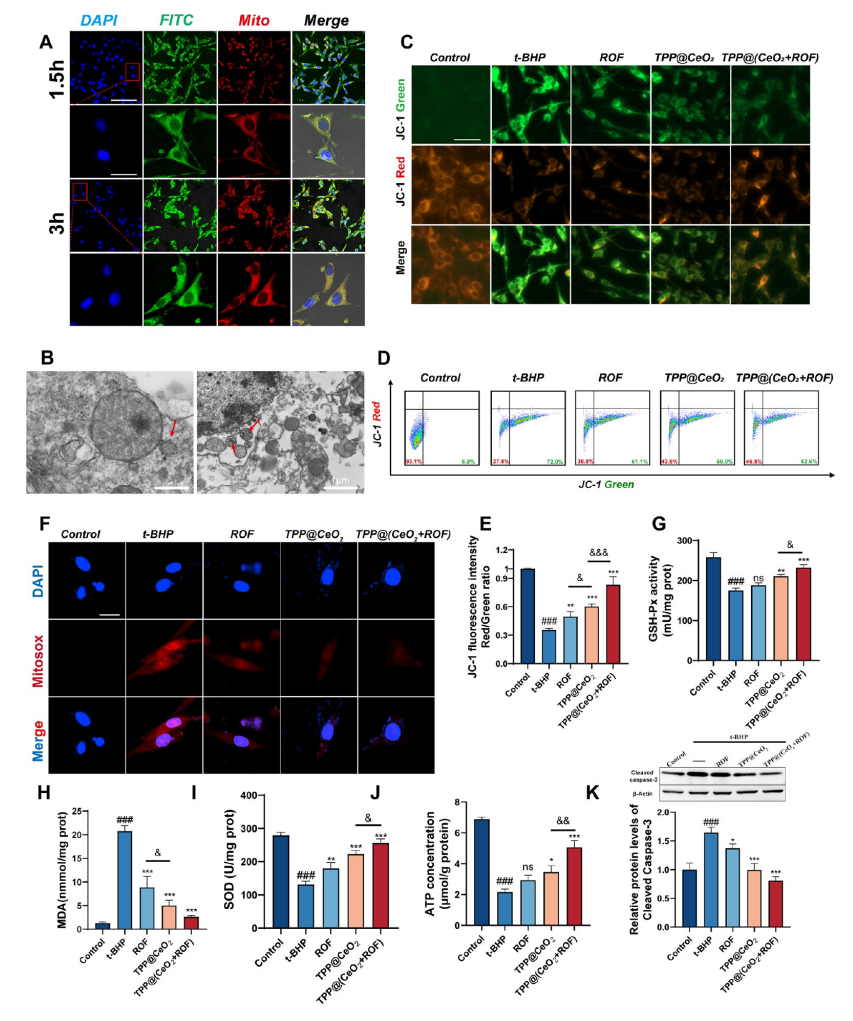
图4.TPP@(CeO2+ROF)调节线粒体功能,抑制t-BHP诱导的细胞凋亡
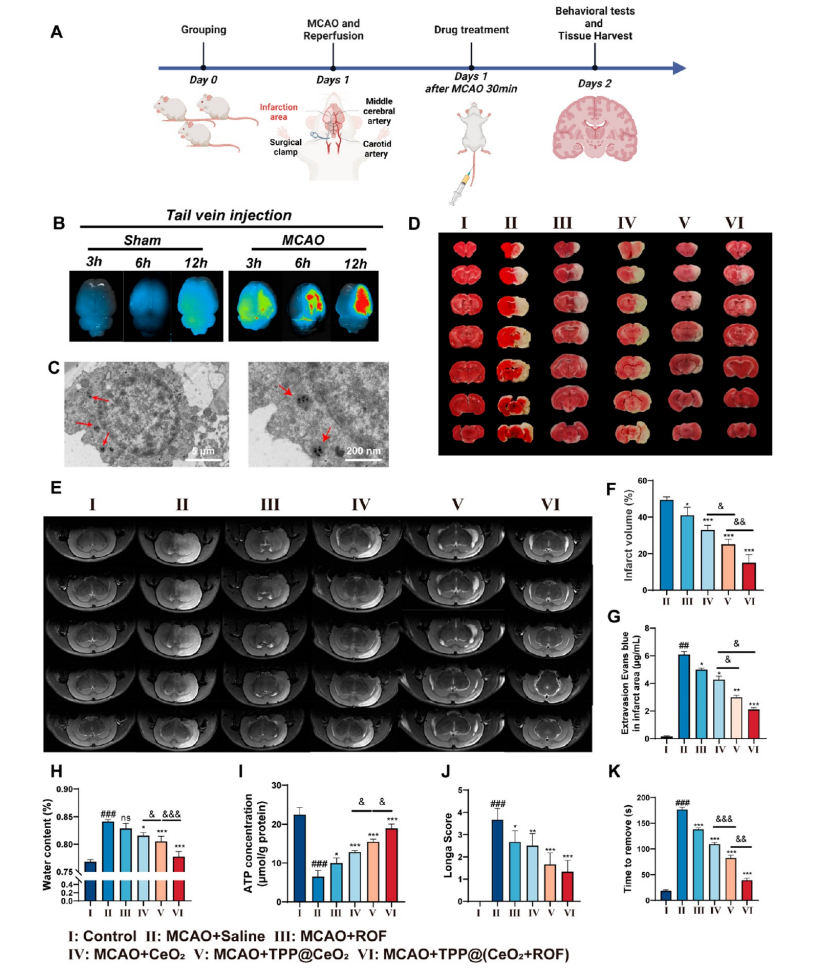
图5.TPP@(CeO2+ROF)对缺血性脑卒中的脑保护作用
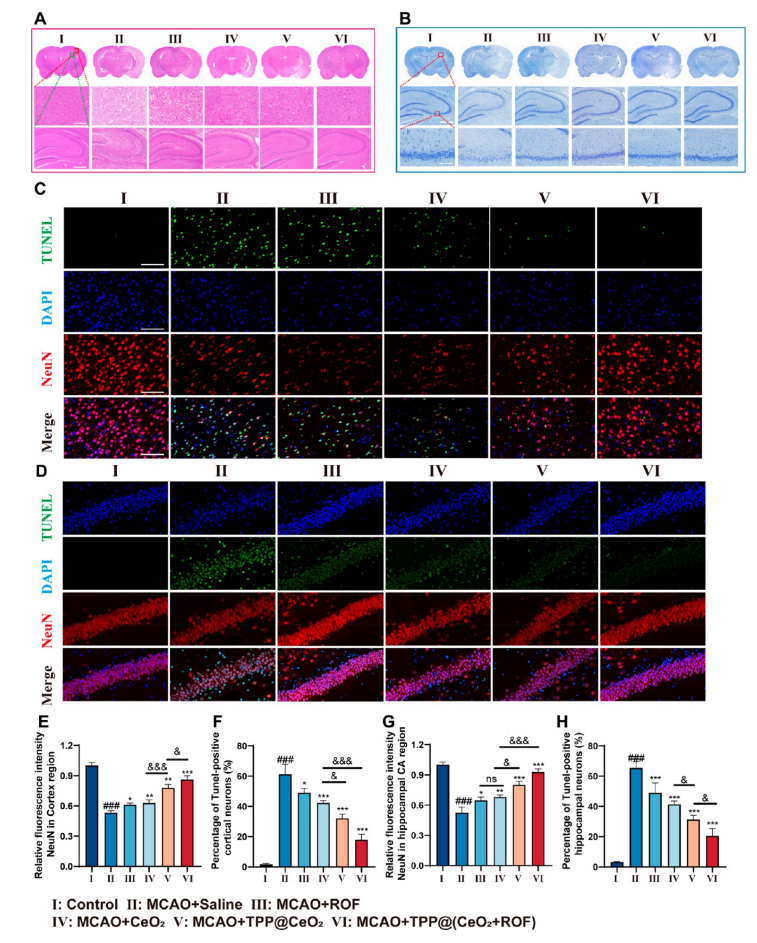
图6.TPP@(CeO2+ROF)对缺血性脑卒中再灌注细胞凋亡的抑制作用
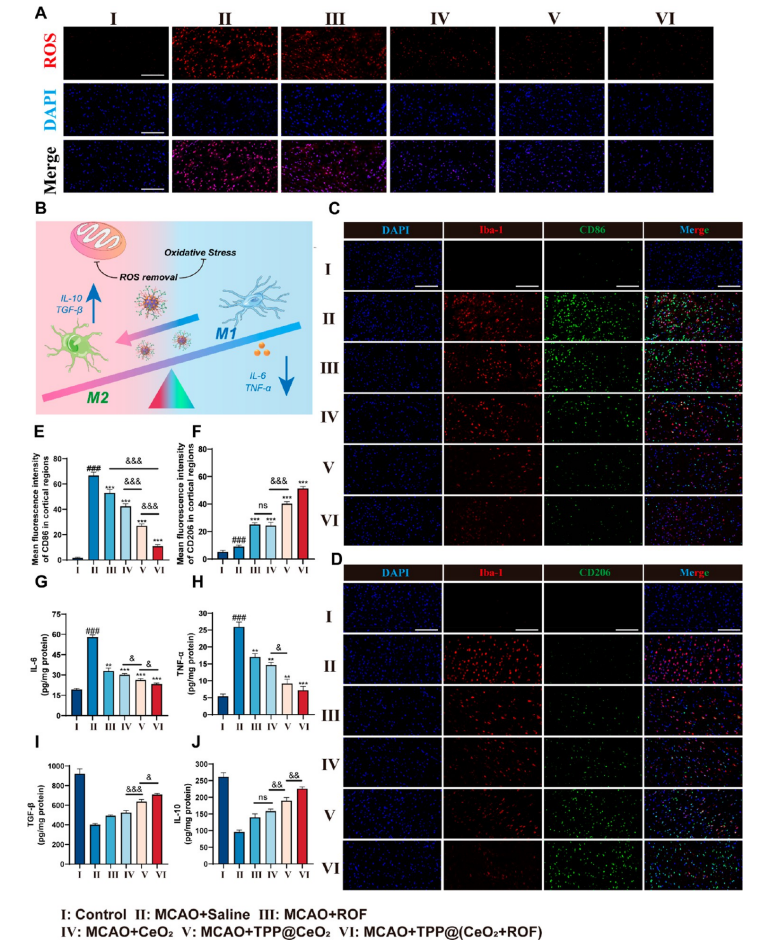
图7.TPP@(CeO2+ROF)纳米颗粒通过逆转胶质细胞表型调节MCAO大鼠的脑炎症水平
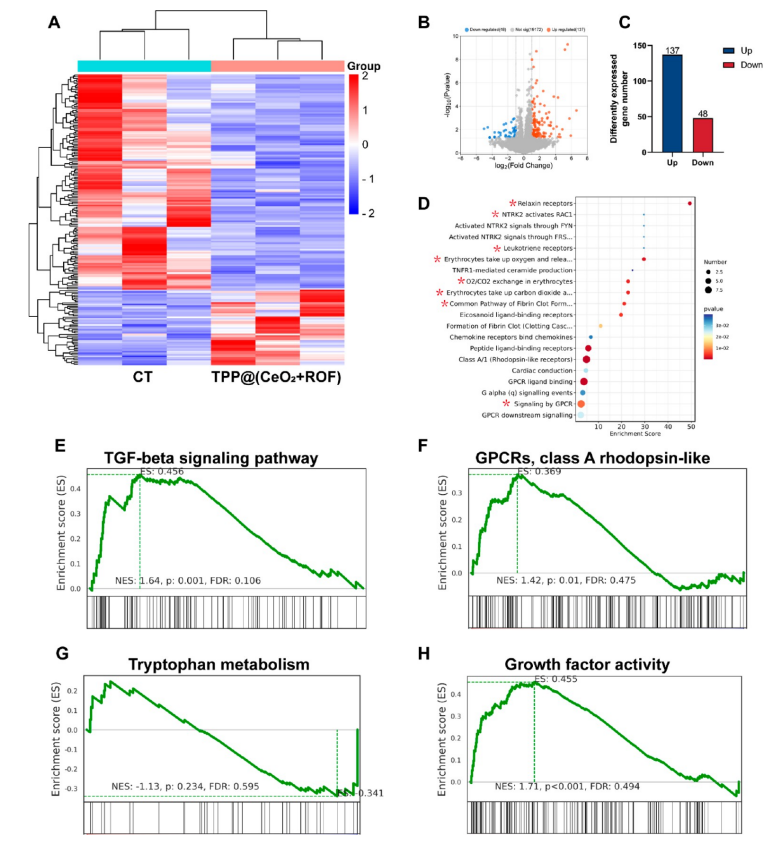
图8.TPP@(CeO2+ROF)处理MCAO大鼠组织的RNA测序分析